<水の科学2>水は、固体、液体、気体に変化する
水には、他の物質にはほとんど見られない、変わった性質があります。
それらについて私たちは「当たり前」と思っていることが多いのですが、マーティン・チャップマン博士(ロンドン南バンク大学名誉教授)によると、水の「常識はずれ」な性質を数えると67 もあるといいます。
まず、水は液体、固体、気体という3 つの状態に変化します。
標準気圧(1気圧)では、温度が0 〜100℃(水の沸点は厳密には99.974℃ですが本稿においては100℃とします) のときは液体です。
そして0℃以下になると氷という固体になります。
反対に100℃で水蒸気という気体になります。
1 つの物質の固体、液体、気体への変化を、日常生活のなかで確認できるのが、水の特徴です。
他の物質は、高温・低温や高圧などの環境を特別な実験室でつくり出さない限り、固体、液体、気体への変化を確認することはできません。
固体、液体、気体の3 つの状態は、物質を構成している粒子間に働く引力の大きさと、粒子の熱運動量の大きさの大小によって決まります。
水は水分子がたくさん集まってできています。
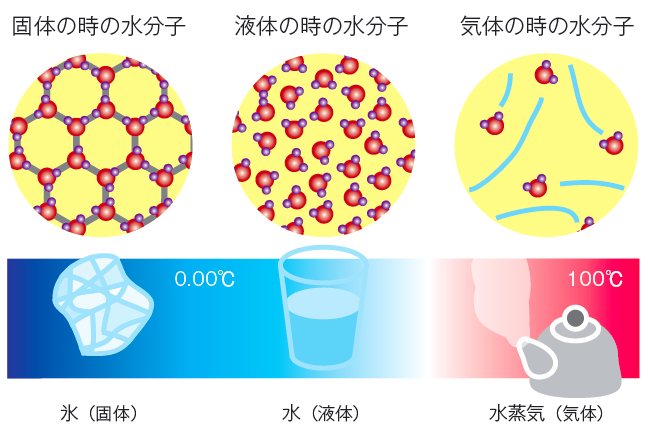
氷のときは、水分子同士の結びつきが強く動きません。水分子同士が互いに接し、相対的な位置は変化しません(その場で振動はします)。
液体の水では、水分子同士の結びつきはゆるくなります。水分子同士は互いに接していますが、相対的な位置は簡単に変化する流体です。一定の形はもたず容器に従うことになります。
水蒸気では、水分子同士の距離が非常に大きく、分子間の引力はほとんどはたらきません。水分子はグループから完全に離れてほぼ自由に運動しています。
