<水の科学5>水の融点・沸点
圧力によって融点・沸点は変わる
1気圧のもとでは、水は100℃で沸騰しますが、気圧が変わると沸騰する温度は変わります。水の状態変化には、温度のほか、圧力が深く関係しています。
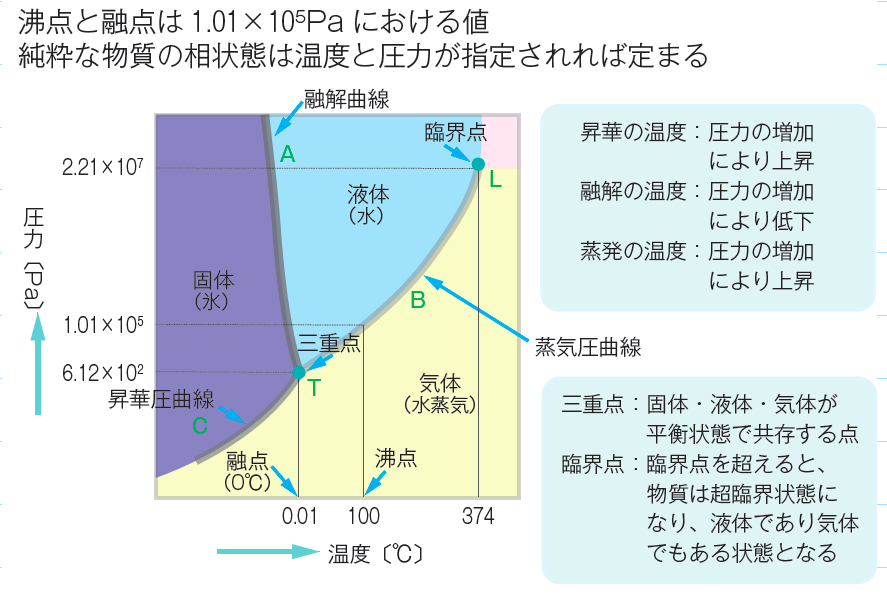
横軸に温度、縦軸に圧力をとり、そのときの状態を表わしたものを状態図といいます。
AT を融解曲線、BT を蒸気圧曲線、CT を昇華圧曲線と呼び、曲線上では両側の物質が平衡して共存しています。
温度、圧力が非常に高くなり、374℃、あるいは2.21 × 107Pa になると、液体と気体の水は互いに区別できなくなり、BT の蒸気圧曲線は終わります。
この点を水の臨界点(L)といい、その温度、圧力を臨界温度、臨界圧力といいます。
一方、T では固体、液体、気体の3つの状態が平衡して共存できます。この点を水の三重点といいます。
なお、ときおり三重点は融点と混同されますが、三重点が氷と水と水蒸気の平衡温度なのに対し、融点は1 気圧のとき飽和している水と氷との平衡温度です。
水の状態図を見ると、BT の蒸気圧曲線の傾きは正になっています。これは圧力が低くなると沸点も低くなる(圧力が高くなると沸点も高くなる)ことを示しています。つまり、高所では気圧が低くなるので沸点は下がります。
たとえば、富士山頂では水は88℃で沸騰します。
高い山にキャンプなどに行くと気圧が低く100℃よりも低い温度で沸騰するのでお米がうまく炊けないことがあります。
反対に高い圧力をかける圧力釜のなかでは沸点が100℃を超えるため、反応速度が100℃のときより速くなり、調理時間が短くなります。
一方、水の状態図のAT の融解曲線の傾きは負になっています。これは圧力が高くなると融点が低くなる(圧力が低くなると融点は高くなる)ことを示しています。
一般の物質では融解曲線の傾きは正で、圧力を増加させると融点が高くなるので、ここでも水は特異な物質だといえます。
この記事へのお問い合せはアクアスフィア・水教育研究所へお願いします。
